
关键词:心力衰竭;中国医学科学院阜外心血管病医院
登记号:CTR20230733
纽卡定(重组人纽兰格林)是由泽生科技自主研发、全球首创的用于治疗包括射血分数降低型心衰(收缩性心衰)、射血分数保留型心衰(舒张性心衰)等疾病的在研重组蛋白药物。其创新作用机制为激活心肌细胞中表达的ErbB2 / ErbB4受体酪氨酸激酶,以调节基因和蛋白表达,促进肌节重组,增加心肌收缩/舒张,逆转心室重构。基于上述科学发现,泽生科技致力于将重组人纽兰格林开发为全球首个通过改善心肌细胞结构和功能治疗慢性心力衰竭的生物药(商品名拟为纽卡定)。
已完成的临床试验显示:纽卡定能够改善慢性收缩性心衰患者心功能,改善长期预后,对心衰患者的死亡风险存在降低趋势,并能大幅降低以NT-proBNP精准确定的特定亚群患者(依据多个大样本量研究和泽生临床数据估算,该目标亚组约占NYHA II-III级收缩性心衰患者的62.5%)死亡率。对三个独立生存获益临床试验的事后亚组分析显示,对目标患者年全因死亡率降低趋势一致、可重复,相对降低幅度均达63.9%-86.1%(其中两项分析单独达统计显著),合并分析显示相对降低73.7%,统计极显著(P=0.0006)。
2020年1月,国家药审中心针对泽生科技附条件上市的申请进行正式批复,要求应继续推进注射用重组人纽兰格林(纽卡定)III 期生存率确证性临床试验 ZS-01-306 研究,目前正在开展一项以心功能为主要疗效指标的三期试验用以支持药物申请附条件批准上市。
适应症:心力衰竭
专业题目:多中心、随机、双盲、标准治疗基础上的安慰剂平行对照评价注射用重组人纽兰格林对慢性收缩性心力衰竭患者心功能及逆转心室重构的影响的 III 期临床试验组长单位:本次临床试验国内主要研究者由 中国医学科学院阜外心血管病医院张健教授牵头,该试验是国内多中心试验,国内有 93 家参研医院。
二、临床试验信息
1.年龄>18岁至75岁,生活自理,能独立行走200m。
2.明确诊断心力衰竭 6 个月及以上,目前病情稳定,NYHA II-III 级,左心室射血分数 (LVEF)≤40%(筛选时心超改良 Simpson’s 法测量值≤40%,且基线时 CMR 测量值≤40%)
3.男性 NT-proBNP≤1700 pg/ml,女性NT-proBNP≤4000 pg/ml (中心实验室罗氏试剂盒检测);NT-proBNP即N端脑钠肽前体。心脏不仅具有泵血功能,而且还具有内分泌功能。B型利钠肽(BNP)由心室分泌并释放入血液。在心衰患者中,由于血容量超负荷导致心室压力增高,此时BNP分泌增加。BNP在受到心肌细胞的刺激后,在蛋白酶的作用下,裂解为NT-proBNP并释放入血液。通过血液可检测到NT-proBNP的浓度从而反映心衰的程度。
4.接受心衰标准基础治疗药物满 3 个月,且 1 个月内未改变心衰治疗药物的种类及剂量;筛选时的实验室检查结果符合研究规定
1.严重室性心律失常;肥心病;严重心脏瓣膜病;先天性心脏病2.基线时左心室收缩末期容积指数(LVESVI)小于 135 ml/m2;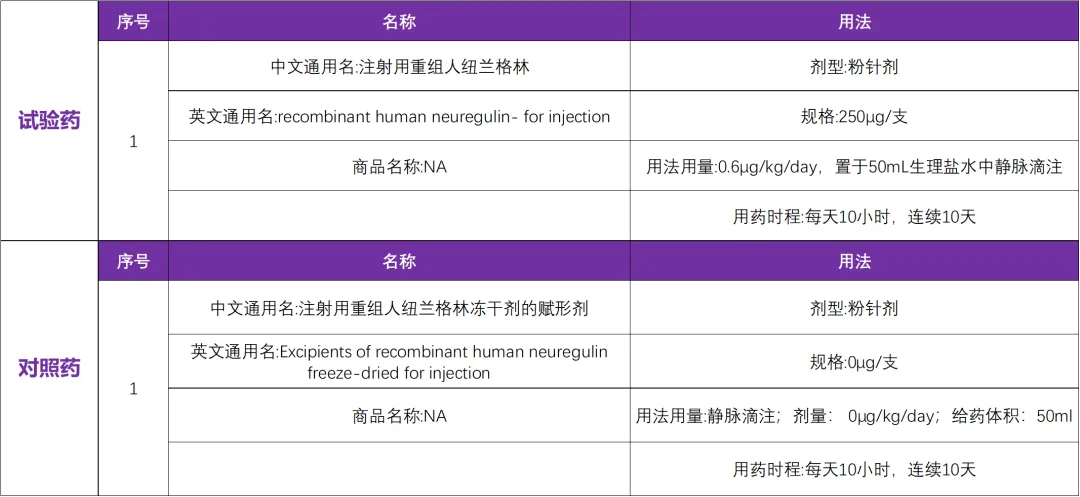
三、参研中心(知名三甲医院)
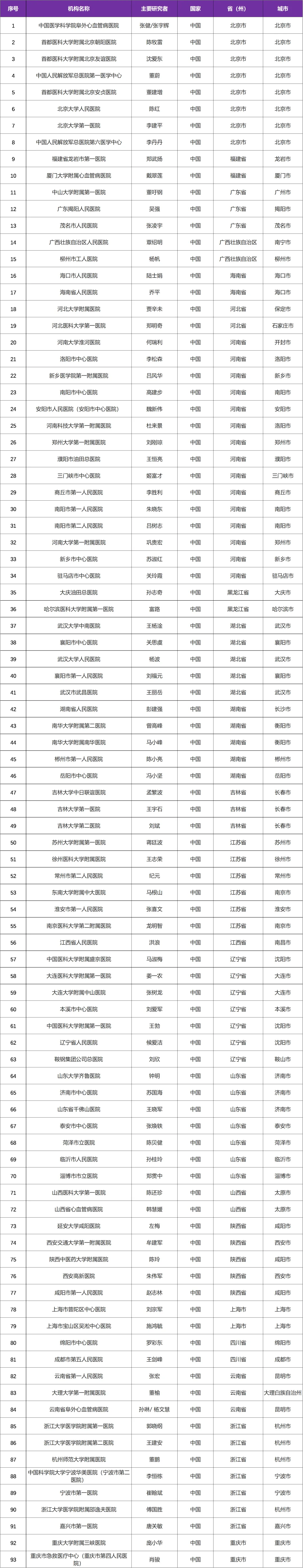
来源:以上信息来自国家药品监督管理局药品审评中心,网址为http://www.chinadrugtrials.org.cn 登记号:CTR20230733 即可查询 I 题图来源:视觉中国
