淋巴瘤是常见的恶性肿瘤之一,每年发病人数约为7.54万,发病率为4.75/10万,死亡人数为4.05万,死亡率为2.64/10万。根据组织病理学改变,淋巴瘤分为霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL),其中NHL发病率约占所有淋巴瘤的90%,约85%的NHL起源于B细胞,而其中最常见的类型是弥漫大B细胞淋巴瘤(DLBCL)。CAR-T疗法是毋庸置疑的,“颠覆者”地位也难以撼动,但价格高也令其尽显“贵族”气质,尤其是国内市场。自2021年中国首个CAR-T疗法——复星凯特阿基仑赛注射液(Yescarta)上市后,很长一段时间以来,“120万”几乎成为CAR-T的代名词。来源:智通财经
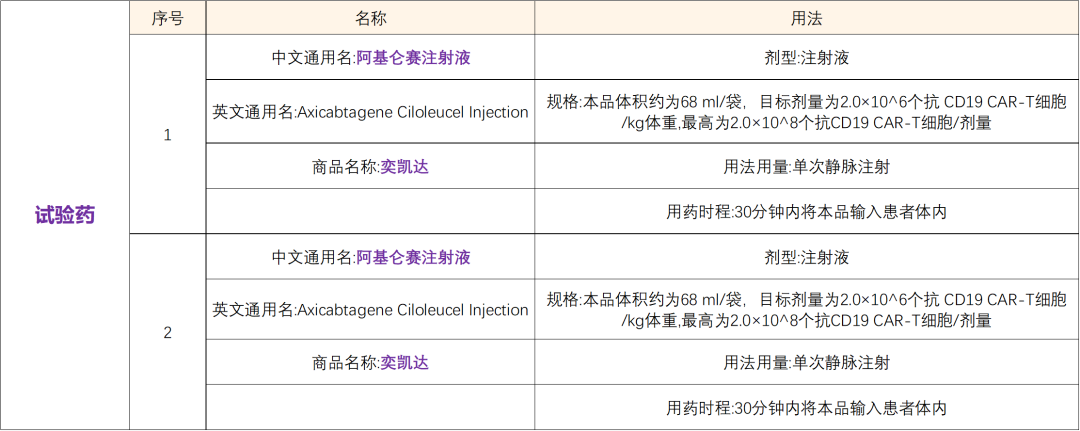
阿基仑赛注射液,是一种自体免疫细胞注射剂,由携带CD19 CAR基因的逆转录病毒载体进行基因修饰的自体靶向人CD19嵌合抗原受体T细胞(CAR-T)制备
2021年6月,国家药品监督管理局通过优先审评审批程序批准复星凯特生物技术有限公司申报的阿基仑赛注射液 (商品名:奕凯达)上市。该药品为我国首个批准上市的细胞治疗类产品,用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者(包括弥漫性大B细胞淋巴瘤非特指型、原发纵隔大B细胞淋巴瘤、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的弥漫性大B细胞淋巴瘤) [1] 。
2022年6月22日,中国首个CAR-T细胞治疗产品奕凯达(阿基仑赛注射液)上市一周年。
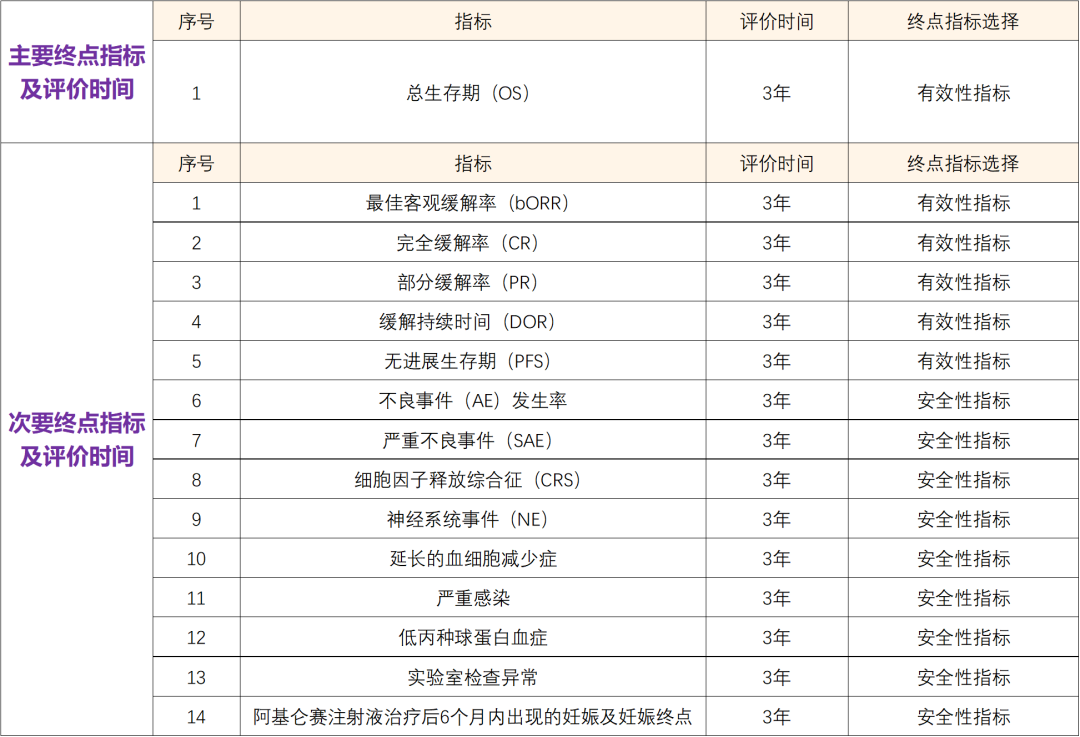
适应症:用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者,包括弥漫性大 B细胞淋巴瘤(DLBCL)非特指型(NOS),原发纵隔大B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡性淋巴瘤转化的DLBCL瘤(说明书获批适应症)通俗题目:评价阿基仑赛注射液治疗复发或难治性非霍奇金淋巴瘤的非干预性临床研究
 信息来源:百度百科
信息来源:百度百科
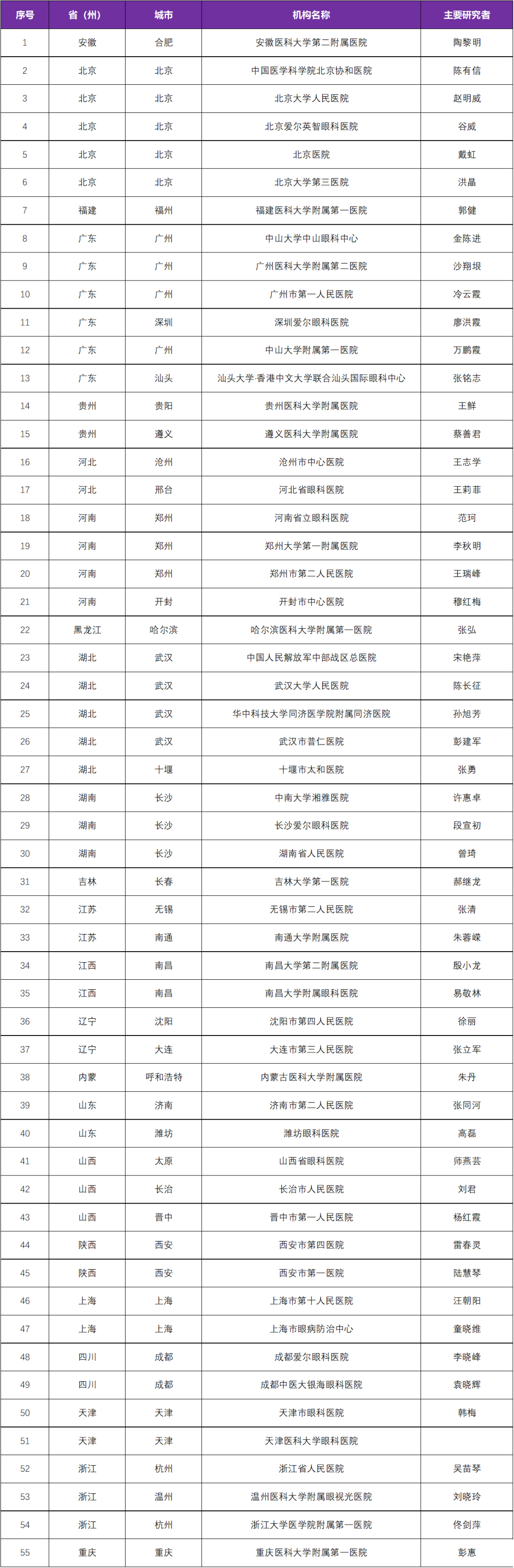
本次临床试验国内主要研究者由 华中科技大学同济医学院附属协和医院胡豫教授、苏州大学附属第一医院吴德沛教授、上海交通大学医学院附属瑞金医院赵维莅教授牵头,该试验是国内多中心试验,参研机构有国内 14 家医院
1.年龄≥18岁,男女不限,ECOG体力评分0或1分2.在中国获得复星凯特商业认证的研究中心接受复星凯特阿基仑赛注射液治疗的复发或难治性非霍奇金淋巴瘤r/rNHL受试者。3.自愿参加本研究并愿意签署知情同意书,对不具有完全民事行为能力的患者,必须获得其监护人的知情书。非随机 开放 单臂试验 国内试验 上市后真实世界研究
三、国内参研医院
以上信息来自国家药品监督管理局药品审评中心,网址为http://www.chinadrugtrials.org.cn
登记号:CTR20211683即可查询
